
Si pudiéramos dividir todo lo que nos rodea en trozos más pequeños hasta llegar al mínimo, ¿qué es lo que tendríamos? La respuesta la podemos encontrar en los átomos y sus distintas partes, pero ni la ciencia ha podido descifrar de forma exacta lo que sucede a un nivel tan pequeño. En cualquier caso, la teoría atómica ha avanzado mucho y esto es lo que sabemos, hasta el momento.
ÍNDICE
¿Qué es un átomo?
El concepto de átomo surgió mucho antes del nacimiento de la física cuántica moderna. En el siglo V a.C, los griegos atomistas, encabezados por Demócrito y Leucipo, propusieron algo llamado la “teoría atómica del universo”. Para ellos, todo lo que nos rodeaba y era perceptible a través de los sentidos estaba formado por pequeñas partículas llamadas átomos. Para ellos, los átomos tenían las siguientes propiedades.
- Son indivisibles, homogéneos e invisibles.
- Solo se diferencian por la forma y el tamaño.
- Las propiedades de la materia cambian en función de cómo están agrupados los átomos.
Aunque esta corriente filosófica no fue vista con buenos ojos, los atomistas no estaban demasiado equivocados. La ciencia ha demostrado que existe esta unidad de materia llamada átomo, pero las propiedades que propusieron no son del todo ciertas. Como podremos comprobar más adelante, los átomos se pueden dividir en partículas subatómicas, por lo que no son indivisibles.
De hecho, la fisión nuclear es el proceso por el cual se divide un núcleo atómico. El proceso de fusionar dos núcleos se denomina fusión nuclear.
Por lo tanto, podríamos describir un átomo como la unidad más pequeña de materia con sus propiedades químicas. Para entender lo pequeño que es un átomo, intenta imagina un metro dividido en diez mil millones de partes. ¿Imposible, verdad? Un átomo es tan pequeño que a la ciencia (con los medios de que dispone actualmente) le resulta muy difícil medir cosas a nivel atómico.
La Real Academia Española ofrece la siguiente definición:
“Partícula indivisible por métodos químicos, formada por un núcleo rodeado de electrones”
Las partes de un átomo
Ahora que tenemos claro el concepto de átomo, pasamos a enumerar las partes y partículas que lo componen.
Las partículas subatómicas
Los electrones son las partículas más ligeras de un átomo y tienen una carga eléctrica negativa. Son partículas elementales, lo que quiere decir que no están formados por partículas más pequeñas o aún no se han descubierto. Otra partícula que forma parte del átomo es el protón, con una carga eléctrica positiva. Por último encontramos los neutrones, que no poseen carga eléctrica. Tanto el protón como el neutrón están, a su vez, formados por quarks, pero nos quedaremos a analizar las partes de un átomo.
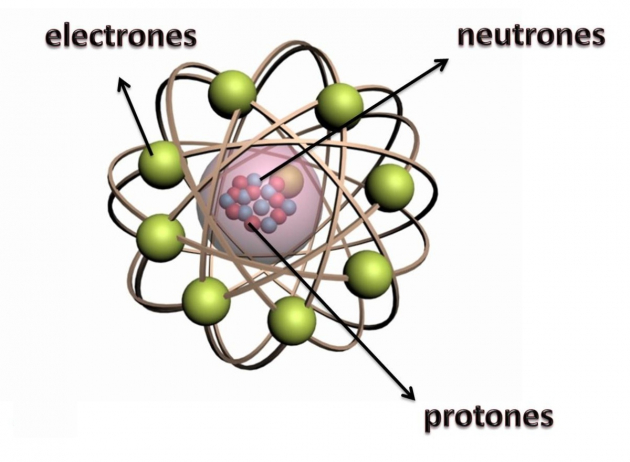
1. El núcleo
Podríamos definir el núcleo como la zona “central” del átomo. En esta parte es dónde los protones y neutrones (este tándem recibe el nombre de nucleones) se mantienen unidos mediante la fuerza nuclear. La fuerza nuclear es la que evita que los protones salgan disparados del núcleo. Antes hemos señalado que los electrones son las partículas más ligeras, por lo que toda la masa del átomo proviene del núcleo.
Si toda la materia que no rodea está formada por átomos de partículas, ¿qué es lo que diferencia a cada elemento? La respuesta es relativamente sencilla: el número de protones que contiene. Alguna vez habrás visto un número junto a cada elemento de la tabla periódica. Ése es el número atómico o número de protones.
2. Nube de electrones
Flotando alrededor del núcleo se encuentran los electrones, que están atraídos por los protones a través de la energía electromagnética. Esta parte también es llamada corteza. Curiosamente, un átomo siempre tiene el mismo número de protones que de electrones, por lo que se dice que son eléctricamente neutros.
Según deducen los científicos, los electrones orbitan alrededor del núcleo siguiendo una órbita circular o elíptica (se les llama capas o niveles electrónicos), al mismo tiempo que giran sobre sí mismos. La capa exterior de electrones también es llamada capa de valencia, y de ellas depende la probabilidad del átomo de producir una reacción química.
Propiedades de un átomo
Por último, repasamos todas y cada una de las propiedades de un átomo.
1. Masa
Como hemos dicho, toda la masa del átomo viene determinada por la cantidad de protones y neutrones que se encuentran el núcleo, y es que los electrones tienen una masa mucho más pequeña. La masa del átomo es tan pequeña que se expresa mediante la unidad de masa atómica (u) o dalton (Da) y su equivalencia en kilogramos sería de 1,660538921 (73) × 10-27
2. Tamaño
Un átomo llega hasta dónde se termina su nube de electrones, pero esa frontera no está siempre clara. Desafortunadamente, no se puede medir el tamaño de un átomo con exactitud, pero podemos hacer una aproximación si tenemos en cuenta un fenómeno físico en el que se ve implicado. Varios estudios señalan que un átomo puede oscilar entre 0,5 y 5 ángstroms (Å), y cada ángstrom equivale a 0.000,000,000,1 metros. Muy pequeño.
3. Propiedades magnéticas
El magnetismo (fuerza de atracción) de cada elemento viene determinado por el movimiento de los electrones alrededor del núcleo, produciendo un campo magnético semejante al de un imán. Esto se ha estudiado mediante la teoría electromagnética, demasiado compleja para exponerla también aquí.
Referencias bibliográficas
Asimov, I., Cruz, A., & Villena, M. I. (1975). Breve historia de la química. Alianza.
Demtröder, W. (2010). Atoms, molecules and photons (p. 194). Heidelberg:: Springer.

